La difracción de rayos X por los cristales es la principal herramienta para el estudio de la estructura atómica y molecular de la materia. Gracias a ella conocemos cómo son las moléculas de los fármacos, de los minerales, de los materiales sintéticos y naturales, y también la estructura de las macromoléculas integrantes de la vida, es decir, los ácidos nucleicos, las proteínas y los carbohidratos. Esta información nos ayuda, por ejemplo, a conocer cómo funcionan los fármacos y a mejorarlos.
¿Quieres saber cuáles son los fundamentos de la difracción? ¿Has oído hablar de las grandes instalaciones de sincrotrón? ¿Sabes cómo se diseña un antibiótico?
Hoy en día conocemos al detalle la estructura molecular de los medicamentos, desde la de la cotidiana aspirina hasta la de los modernos fármacos diseñados para combatir el sida: aquí un carbono y aquí, a tanta distancia, otro; y este oxígeno está a su izquierda girando 112º, etcétera. Así, podemos construir modelos de las moléculas como construimos modelos a escala de barcos o de aviones. Esa información estructural a nivel atómico revolucionó para siempre la mineralogía, la química, la farmacología, la bioquímica, la medicina y la ciencia de los materiales. Esa información tan valiosa se la debemos a la cristalografía.
El poder de la nueva técnica de difracción de rayos X por los cristales para desvelar la estructura de los minerales asombró al mundo científico. Era una información importante para entender las propiedades de los minerales, la reactividad de los compuestos químicos y en último término, relacionar la estructura de los compuestos farmacológico con sus propiedades terapéuticas, y las de las moléculas biológicas con la función que realizan en el organismo.
La difracción de rayos X se convirtió así en el más potente “microscopio” disponible por la ciencia, el único capaz de ver la estructura molecular de los cristales. Obviamente era imprescindible tener cristales del compuesto. Primero se usaron minerales, los cristales que la naturaleza ofrecía. Al final de los años 20 ya se establecieron la estructura de sulfuros, de granates y de silicatos, compuestos con pocos átomos diferentes. Y también se descubrieron las estructuras de importantes aleaciones metálicas.

Un granate (izquierda) y su estructura (derecha).
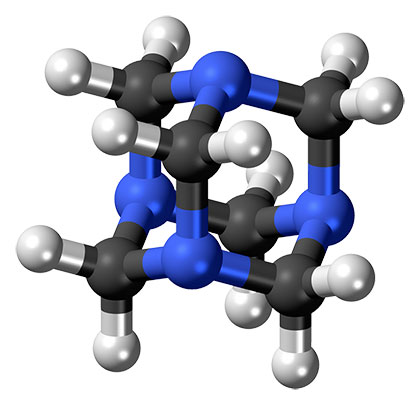
Pronto se empezaron a estudiar compuestos que había que cristalizar. El primer compuesto orgánico cuya estructura se resolvió por difracción de rayos X fue la hexametilentetramina. Obviamente era una estructura sencilla con cuatro átomos de nitrógenos (en azul) seis carbonos (en negro) y doce hidrógenos (en gris).
Resolver estructuras de moléculas cada vez más complejas y más interesantes era un reto imparable. Dorothy Hodking se destacó por determinar la estructura tridimensional de los primeros compuestos de interés bioquímico, como el colesterol en 1937, la penicilina en 1945, la vitamina B12 en 1954 y la insulina en 1969. En 1964 recibió el Premio Nobel por sus investigaciones.
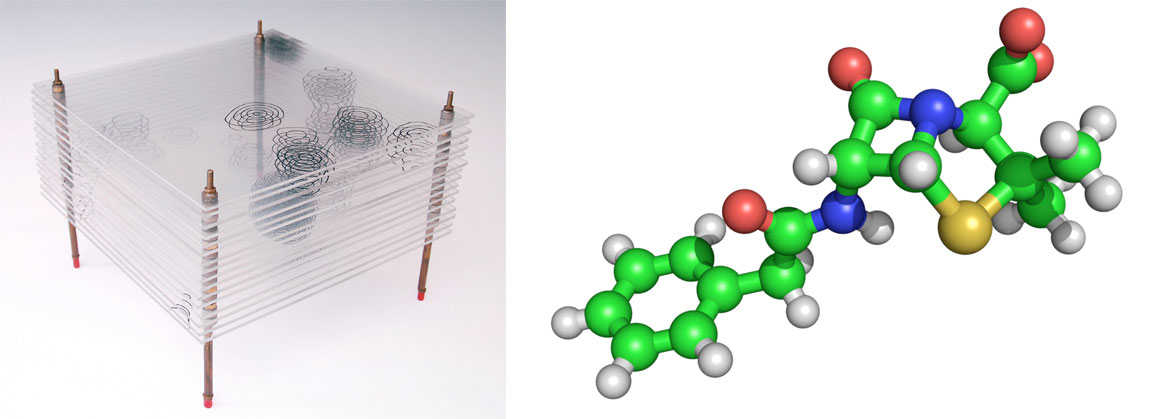
Izda: Modelo de la estructura de la penicilina por realizado por Dorothy Hodgkin. Dcha: La estructura molecular de la penicilina. Cada color representa un tipo de átomo. El verde el carbón, el rojo el oxigeno, el blanco el hidrogeno, el azul el nitrógeno y el amarillo el azufre.
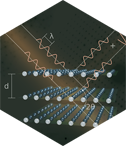
En 1925 Louis de Broglie recibió el Premio Nobel de Física por su descubrimiento de la naturaleza ondulatoria de los electrones. La idea de usarlos en difracción complementando a los rayos X estaba servida. Pronto se descubrió que los haces de electrones también son difractados por los cristales. La física en la que se basa esa difracción es diferente de la de los rayos X pero los patrones que producen los haces difractados son y se interpretan de la misma forma. Por ese descubrimiento, Clinton Joseph Davisson y George Paget Thomson recibieron el Premio Nobel de Física en 1937.

Izda: Louis de Broglie. Dcha: Diagramas de difracción de electrones.
Plus ultra. Había que ir más allá. Estructuras más complejas, más grandes y con un mayor número de átomos diferentes. Pero había un escollo que parecía insalvable para entender completamente toda la información que contenían esas manchas negras distribuidas armónicamente en la placa fotográfica. El llamado problema de las fases.
La información molecular estaba ahí, en esos puntos, de cuyo tamaño y negrura podíamos obtener la intensidad, es decir la amplitud, pero no la otra información que contiene una onda, la fase. Era como recomponer una sinfonía a partir de una partitura en la que falta la numeración de compases, por lo que es imposible sincronizar el piano con las cuerdas en las que también tenemos «desfasado» cada uno de los violines, violas y violonchelos… Solo podremos apreciar la sinfonía cuando «alineemos» temporalmente las partituras, es decir, cuando las pongamos «en fase». Durante mucho tiempo, el problema se consideraba no solo difícil, sino insoluble. Pero Herbert Hauptman y Jerome Karle lograron encontrar las ecuaciones que lo desgranaban y el método para resolverlas directamente. E Isabella Karle fue quien convirtió esas ideas en un protocolo experimental. Así, pusieron a disposición de los químicos y bioquímicos la herramienta que les permite soñar con entender las reacciones y la vida a nivel molecular: la determinación de la estructura real de las moléculas. Por esa admirable contribución a lo que se llamó los métodos directos de resolución de estructuras, Herbert Hauptman y Jerome Karle recibieron el premio Nobel de Química en 1985.

Izda: Jerome and Isabella Karle. Dcha: Herbert Hauptman.
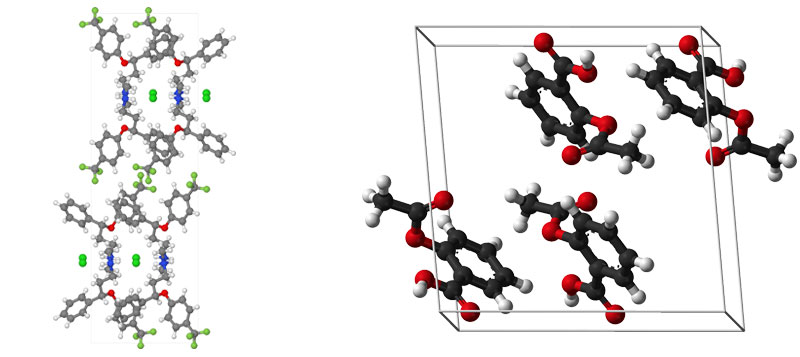
Izda: La fluoxetina (conocida como Prozac, su primer nombre comercial) es un antidepresivo indicado para tratar los trastornos depresivos mayores, el trastorno bipolar, el trastorno obsesivo-compulsivo, la bulimia nerviosa. En 2012 se descubrió que también es un potente antiviral.. Dcha: El ácido acetilsalicílico, conocido popularmente como aspirina, es un fármaco de la familia de los salicilatos, usado frecuentemente como antiinflamatorio, analgésico. Su consumo mundial es de 25 millones de kilos al año. La molécula está formada por nueve átomos de carbono (en negro), ocho de hidrogeno (en gris) y cuatro de oxígeno (en rojo) pero su disposición en el espacio como muestra la figura no se descubrió hasta 1964..
¿Sabías que…?
- La cristalografía ofrece a los científicos un conocimiento útil de la estructura de las proteínas y a partir de allí, pueden desarrollar experimentos para crear nuevos fármacos. La técnica más usada para el estudio de farmacos a nivel molecular es el «Docking», que consiste en calcular, a partir de la estructura cristalográfica del principio activo y de la molñécula «diana terapeútica», donde y con que orientación interaccionarán. Conocer esta interacción es fundamental para el diseño racional de fármacos.
- La huella cristalográfica de un fármaco es, como su carnet de identidad, única, permanente e intransferible. Si la huella de una muestra es diferente de la conocida, estamos ante un medicamente adulterado.
- El desarrollo de los fármacos modernos, de la nanotecnología y de la biotecnología se basa en los resultados cristalográficos. Las propiedades de las formas sólidas de los ingredientes farmacológicos activos depende, en gran medida, de su estructura interna.
- Dorothy Hodgin usó la difracción de RX para descubrir no sólo la estructura de la penicilina sino también la de la vitamina B12, y más tarde la de la insulina.
Para saber más…
- Conoce un poco más sobre Dorothy Hodgkin, pionera en la técnica de determinación de estructuras de sustancias de interés bioquímico mediante RX.
- Si quieres saber a qué se didica la biomedinia consulta esta página.
- Puede leer más sobre el papel de la cristalografía en el desarrollo de fármacos en esta página o en este artículo.