03 Cristales: materia ordenada
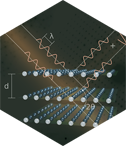
La característica que define a los cristales y los diferencia del vidrio es el orden. Los cristales son la materia ordenada. Están construidos como un apilamiento ordenado de átomos o de moléculas o de conjuntos de átomos y moléculas. Siempre existe en ellos una unidad, la llamada celda unidad, que puede ser un átomo, una molécula o un conjunto de átomos o moléculas, que se repite periódicamente en el espacio rellenando un volumen.

El orden periódico, la periodicidad, es una de las propiedades fundamentales de un cristal. No le será difícil entender este concepto de materia periódicamente ordenada. Lo vemos en solerías, en el empapelado de las paredes o en los muros de ladrillos de las casas. Lo usamos siempre que queremos cubrir una superficie. Por ejemplo un muro de ladrillos. En este muro la distancia entre cada bloque o ladrillo es siempre la misma. Esa distancia se llama periodo y como puede ver cambia con la dirección. A esa propiedad de la materia así ordenada se le llama periodicidad. Así de fácil.

Esos ladrillos son el equivalente a lo que llamamos celda unidad cristalográfica. Para crear una estructura cristalina solo tiene que imaginarse convertir esos ladrillos en unidades moleculares. Le vamos a ayudar a imaginar cómo hacerlo convirtiendo cada ladrillo cúbico de un juego de construcción por la unidad repetitiva de un cristal molecular.
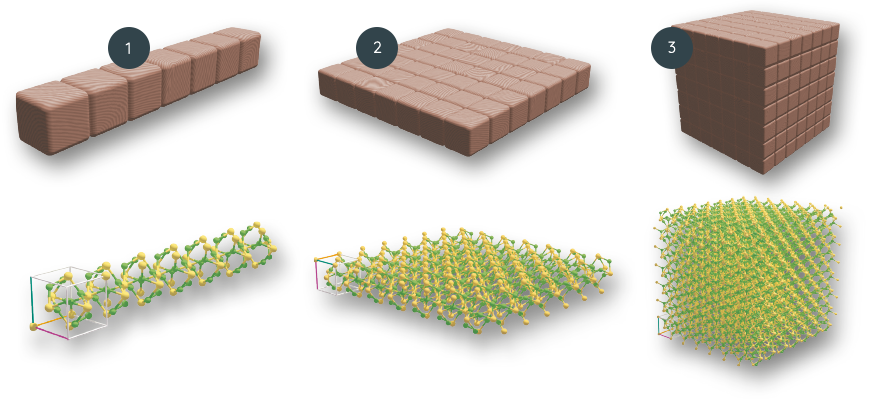
Si colocamos bloques o celdillas uno junto a otro formando una fila tendremos una distribución periódica en una dirección (1).
Si empaquetamos varias de estas filas en la dirección perpendicular tendremos un plano periódico en dos direcciones. Esto es un cristal bidimensional (2).
Finalmente, si apilamos bloques o celdillas unidad en la tercera dirección, tendremos un apilamiento tridimensional periódico de elementos idénticos (3).
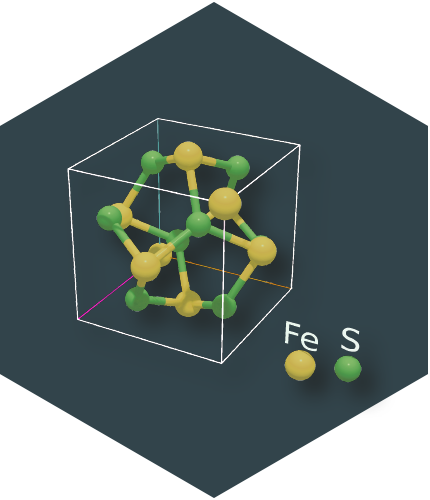
La celda unidad que hemos elegido es la de la pirita, un sulfuro de hierro muy común, un mineral muy bonito de color dorado.

Así están construidos los cristales. La única diferencia es que un cristal de un centímetro de pirita contiene alrededor de 100.000.000.000.000.000.000.000 celdillas unidad en vez de las trescientas cuarenta y tres de la ilustración.
Ahora, imagínese que se encuentra en el interior de esa estructura cristalina. Colóquese en un átomo de hierro y mire su entorno. Muévase al mismo átomo de hierro de otra celda y verá que su entorno es el mismo. Esa es otra propiedad de los cristales: la homogeneidad.
Ahora trate de desplazarse en una dirección determinada. Tendrá que sortear con dificultades los enlaces que unen a los átomos. Párese y cambie la dirección de movimiento. Verá que la dificultad de moverse ha cambiado también. Esa es otra propiedad importantísima de los cristales: la anisotropía.
Una de las características más llamativas de los cristales es su belleza poliédrica. Son sólidos con una morfología limitada por caras planas y aristas rectas que se unen en vértices puntiagudos. La pirita, ese mineral cuya estructura acabamos de crear, se encuentra en la naturaleza en forma de bellos cristales con distintas formas. Vamos a mostrarle que todas ellas son una consecuencia de la periodicidad interna del cristal.

Los cubos de pirita son muy sencillos de crear por apilamiento de los bloques o celdas unidad de forma que delimiten un cubo tridimensional con seis caras perfectamente planas (1).
Pero si permitimos que las caras puedan ser escalonadas, entonces pueden formarse otras caras diferentes. Recuerde los millones de bloquecitos idénticos que forman los cristales. Aunque en detalle las caras estén escalonadas, esos escalones serían imperceptibles a la vista humana. Por ejemplo, si hacemos que las caras del cristal sean perpendiculares a los vértices de la celda unidad, la forma cristalina resultante es el octaedro (2).
Si hacemos que las caras externas del cristal sean perpendiculares a las aristas del cubo tenemos otro tipo de cara, el pentagonododecaedro (3).
El que un mineral cristalice con una u otra forma o con combinaciones de ellas depende de las condiciones de cristalización. Los ángulos que forman las diferentes caras de un cristal dependen exclusivamente de las dimensiones de la celda unidad, por lo que son siempre constantes para un determinado compuesto. Es lo que se llama la ley de constancia de los ángulos de un cristal.
En la naturaleza existen más de cuatro mil minerales distintos, es decir, cuatro mil distintas estructuras cristalinas. Y cientos de miles de otras estructuras cristalinas han sido y siguen siendo obtenidas cristalizando en el laboratorio productos naturales y compuestos de nueva síntesis. Todas esas cientos de miles de estructuras se pueden clasificar en 230 grupos distintos gracias a otra propiedad fundamental de los cristales: la simetría.